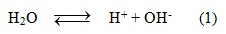Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit-bazo - Hóa Học 11
Học xong bài này các em sẽ đánh giá được độ axit và kiềm của các dung dịch. biết được màu sắc của 1 số chất chỉ thị trong dung dịch ở các khoảng ph khác nhau
Bạn phải là thành viên VIP mới được làm bài này! Đăng ký mua thẻ VIP tại đây
Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit-bazo
I. Nước là chất điện li rất yếu
1. Sự điện li của nước
Nước điện li rất yếu:
2. Tích số ion của nước
- Môi trường nước là môi trường trung tính
- Tại 25oC nước có nồng độ:
[H+] = [OH-]= 1,0.10-7 (mol/l)
- Đặt KH2O= [H+]. [OH-]= 1,0.10-7 x 1,0.10-7= 1,0.10-14
- KH2O được gọi là tích số ion của nước. Ở nhiệt độ xác định, tích số này được coi là hằng số ở trong nước tinh khiết và một số dung dịch loãng khác.
3. Ý nghĩa tích số ion của nước
a) Môi trường axit
- Khi hòa tan axit vào nước, nồng độ [H+] tăng vì vậy nồng độ [OH-] phải giảm sao cho tích số ion của nước không đổi
- Vậy môi trường axit là môi trường trong đó:
[H+] > [OH-] hay [H+]>1,0.10-7 M
b) Môi trường kiềm
- Khi hòa tan bazo vào nước, nồng độ [OH-] tăng vì vậy nồng độ [H+] phải giảm sao cho tích số ion của nước không đổi
- Vậy môi trường kiềm là môi trường trong đó:
[H+] < [OH-] hay [H+]< 1,0.10-7 M
Như vậy, độ axit và độ kiềm có thể được đánh giá chỉ bằng nồng độ H+:
+ Môi trường trung tính: [H+]=1,0.10-7 M
+ Môi trường axit: [H+]>1,0.10-7 M
+ Môi trường bazo [H+]< 1,0.10-7 M
II. Khái niệm về chất chỉ thị axit bazo
1. Khái niệm về pH
- Để đánh giá độ kiềm và độ axit người ta dựa vào nồng độ H+
- Để tránh ghi nồng độ H+ với số mũ lớn người ta dùng giá trị pH quy ước:
[H+]= 10-pHM. Nếu [H+] = 10-aM thì pH=a
Ví dụ: [H+] = 1,0.10-2M => pH= 2: Môi trường axit
[H+] = 1,0.10-7M => pH= 7: Môi trường trung tính
[H+] = 1,0.10-9M => pH= 9: Môi trường bazo
- Thang pH thường có giá tị từ 1 đến 14
2. Chất chỉ thị axit bazo
- Chất chỉ thị axit bazo là chất có màu biến đổi phụ thuộc vào giá tị pH của dung dịch
- Khi trộn lẫn một số chất chỉ thị có màu biến đổi kế tiếp nhau theo giá trị pH ta thu được chất chỉ thị vạn năng